河南美凯生物科技有限公司
总 机:0395-3333801
客 服:0395-3333802
人事部:15303957929
邮 箱:3176821628@qq.com
邮 编:462000
网 址:www.maincare.cn
地 址:漯河市源汇区创业路与南环路西北角
周边公交:126、202、102路车
本指南规范了临床实验室进行血细胞分析(全血细胞计数、白细胞分类及外周血细胞形态学分析)的报告质量要求,由国内血细胞分析领域的多名专家结合国内外相关行业标准和共识共同完成,旨在为临床检验人员对全血细胞计数和白细胞五分类尤其是其异常结果的复检、审核及报告提供参考。
本指南着重于统一以下内容:
①标本存在血细胞分析干扰因素,需要进行特殊处理时的报告方式;
②血细胞分析发现异常细胞或病原生物等情况时的报告方式。
已有文献对检验报告的格式、结构及发布方式等给出了较为详细的通用要求,这里不再赘述。
一、血细胞分析报告内容
(一)数值报告
1. 红细胞相关参数:
至少报告红细胞计数(red blood cell count,RBC)、血红蛋白(hemoglobin,Hb)、血细胞比容(hematocrit,Hct)、平均红细胞体积(mean corpuscular volume,MCV)、平均红细胞血红蛋白含量(mean corpuscular hemoglobin,MCH)及平均红细胞血红蛋白浓度(mean corpuscular hemoglobin concentration,MCHC)。具有临床价值的其他相关参数亦推荐报告,如红细胞体积分布宽度(red blood cell volume distribution width,RDW)等。
2. 白细胞相关参数:
至少报告白细胞计数(white blood cell count,WBC)及成熟白细胞分类计数的绝对值和百分数,如中性粒细胞(neutrophil,Neut)、淋巴细胞(lymphocyte,Lymph)、单核细胞(monocyte,Mono)、嗜酸性粒细胞(eosinophil,Eos)、嗜碱性粒细胞(basophil,Baso)。病理情况下出现异常细胞需进行形态学检查以纠正仪器测定的白细胞分类计数结果时,推荐报告形态学检查结果。形态学白细胞分类计数时,需进行白细胞分类鉴定并报告的细胞类型还应包括原始细胞(blast)、异常早幼粒细胞、各阶段幼稚粒细胞、反应性淋巴细胞和异常淋巴细胞,以及不能识别的细胞等。
形态学白细胞分类计数时,如见到有核红细胞(nucleated red blood cell,NRBC),应以“NRBC:XX个/100WBC”的格式报告 NRBC 的数量,必要时报告分化阶段;如见到小巨核细胞或裸核巨核细胞时,应予以提示,均不纳入白细胞分类计数。
3. 血小板相关参数:
至少报告血小板计数(platelet count,PLT)。具有临床价值的其他相关参数亦可报告,如平均血小板体积(mean platelet volume,MPV)等。
(二)描述性报告
1. 报告内容:
数值异常可不予描述,但需在数值报告中给予相应的提示。在描述性报告中,应着重对具有临床意义的血细胞形态信息尤其是异常血细胞形态给予描述。标本异常时,对存在的干扰因素和必要的处理应给予相应描述,并说明哪些指标无法准确检测。干扰因素主要有:溶血、冷凝集、乳糜、黄疸、血小板聚集、冷球蛋白、有核红细胞、难溶红细胞以及数量较多的巨、大血小板等。干扰因素中未包含血液凝固、稀释、采集量过多/过少、放置时间过长、运输及储存不当等情况。对于采集量过多/过少等标本如需采取让步检验,亦应在报告中给予适当描述说明。
2. 报告层次:
建议分为 3 个层次:
层次1,对观察到的异常形态进行简明规范的综合描述,避免使用模糊术语;
层次2,视情况提出可能的诊断或排除诊断的建议;
层次3,在层次1 和层次2的基础上,视情况提出下一步需进行的检查或采取的措施。
3个不同的报告层次并不是强制必须的,根据具体情况可对报告层次进行调整。
二、异常标本的识别、处理及报告
异常标本包括但不限于以下情况。
1. 溶血标本:
无论是体内还是体外溶血标本,严重时均可导致MCH及MCHC假性增高,红细胞碎片亦可干扰PLT检测结果。对于溶血标本,应首先判断溶血的程度及性质以决定是否需按照不合格标本处理。体内溶血标本以及体外溶血可采取让步检验的标本,血小板计数应采用可排除细胞碎片干扰的方法进行检测,并描述:“溶血标本,红细胞相关参数检测结果仅供参考”。
2. 冷凝集标本:
红细胞凝集可使得RBC以及Hct假性减低,从而导致MCHC、MCH以及MCV假性增高,亦可能影响 WBC 检测结果。对于冷凝集标本可将其放置37 ℃温育至少30 min直至肉眼无可见的凝集后立即上机检测;对于使用温育法无法纠正的重度冷凝集标本,可行温育后稀释或血浆等量置换法重新检测;经血涂片复检未发现其他异常后方可发出报告。报告描述:“可见红细胞凝集现象,此结果为温育和/或稀释和/或血浆等量置换后纠正结果,仅供参考”。血浆等量置换法可对RBC等参数进行纠正,但对其他参数检测结果可能会产生影响,故需操作规范、吸样准确,PLT等参数宜参考首次检测结果。
3. 乳糜血标本:
乳糜血标本常引起Hb、MCH、MCHC及电阻抗法PLT等测定结果假性增高,PLT宜采用替代方法进行确认,Hb、MCH、MCHC等结果宜在标本进行血浆等量置换后复测红细胞相关检测结果给予纠正;并描述:“乳糜血标本,此结果为纠正后结果,仅供参考”。
4. EDTA抗凝引起的血小板假性减低标本:
对高度怀疑由EDTA诱导的血小板聚集引起PLT假性减少的标本,可更换抗凝剂重新采集静脉血复查PLT;对于采用枸橼酸钠抗凝管(抗凝剂和采血量比例为1∶9)复查PLT的标本,红细胞及白细胞相关参数采用EDTA抗凝静脉血的检测结果,PLT为枸橼酸钠抗凝管的检测结果×1.1;并描述:“EDTA抗凝血中血小板呈聚集状态,PLT为枸橼酸钠抗凝血纠正结果,仅供参考”。此外,干扰WBC时亦需要给予适当纠正。二次采血有难度或更换抗凝剂仍然无法纠正的标本,亦可以选取如下方式进行处理:
①37 ℃温育、涡旋震荡器高速震荡法或是加入阿米卡星/硫酸镁进行解聚后上机检测,
②使用已验证具有血小板解聚功能的血液分析仪进行检测,
③仪器旁采集非抗凝静脉血或末梢血标本立即上机检测,
④采集非抗凝末梢血直接用血小板稀释液稀释后进行显微镜计数。
5. 冷球蛋白干扰标本:
冷球蛋白通常干扰血液分析仪对血小板计数和(或)白细胞计数的测定,血涂片中有较多的冷球蛋白存在时,可将标本 37 ℃温育30min后立即上机检测;或采用其他不受干扰的测定方法如荧光染色的方法或流式细胞分析法等进行检测;亦可采用手工计数法进行显微镜计数,必要时进行形态学白细胞分类计数;结果纠正后方可发出报告,并描述:“镜下可见疑似冷球蛋白,血小板和白细胞计数为纠正后结果,仅供参考”。
6. 有核红细胞增多标本:
有核红细胞增多常干扰血液分析仪对WBC的测定。若血液分析仪缺少有核红细胞检测通道或试剂尚不能自动纠正
NRBC对WBC检测结果的干扰,当血涂片中发现每100个白细胞中有5个及以上NRBC时需对白细胞计数进行校正。校正公式如下:
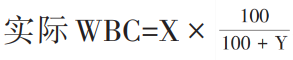
式中 X 为校正前 WBC(或外周血有核细胞总数)、Y为分类100个WBC过程中所见有核红细胞数。
对有干扰因素的标本,如采用特定标志对干扰项目进行了识别处理,亦可在报告中予以提示。
三、异常血细胞形态报告
异常血细胞形态报告宜采用分级报告模式,应着重报告有临床诊断和鉴别诊断意义的形态学信息。分级报告可采用双层报告,即程度和(或)百分比,程度包含“1+(轻度)”“2+(中度)”和“3+(重度)”3 个等级。通常情况下,异常血细胞形态达“2+”和“3+”时给予报告,但因少量的裂片红细胞(schistocyte)在弥散性血管内凝血(disseminated intravascular coagulation,DIC)、血栓性血小板减少性紫癜(thrombotic thrombocytopenic purpura,TTP)和溶血性尿毒综合征(hemolytic uremic syndrome,HUS)等疾病的诊断和监测中具有一定的临床意义,故裂片红细胞为“1 +(少量/稀有)”时也应报告。
(一)红细胞
1. 建议根据分级报告模式对大多数红细胞异常形态给予分级报告,但裂片红细胞应计数百分比(表1)。

2. 应至少评估1000个红细胞中形态异常红细胞的百分比,并注意排除推片等因素的影响。
3. 新生儿出生后1周内外周血中出现有核红细胞属于生理情况,其他情况下外周血中出现有核红细胞常属于病理状态,应给予计数并适当描述。如仅为单纯的有核红细胞增多或伴有红细胞异常,应结合网织红细胞计数等,判断是否需进行溶血相关筛查。
(二)白细胞
在进行血涂片白细胞形态学分类时,通常计数100个白细胞,当见到原始细胞等异常细胞时建议计数200个白细胞。描述性报告多集中于细胞的形态异常以及外周血中出现幼稚细胞、原始细胞等情况。
1. 成熟中性粒细胞
杆状核中性粒细胞作为成熟中性粒细胞,在分类计数时与分叶核中性粒细胞一并以“中性粒细胞”进行分类计数报告。当杆状核中性粒细胞>5%时,提示存在核左移现象,应给予适当描述说明。其他可能需要描述的异常形态见表2。
2. 幼稚粒细胞
建议详细分类计数早、中、晚幼粒细胞。在描述性报告中,层次1需对血涂片中出现幼稚粒细胞进行描述说明,必要时对伴有的其他异常进行描述;怀疑有血液系统肿瘤时如慢性髓系白血病(chronic myeloid leukemia,CML)、慢性粒单细胞性白血病(chronic myelomonocytic leukemia,CMML)等,在层次2中应给予相应提示;层次3对进一步诊断需要做的检查提出建议,如骨髓细胞学、细胞遗传学或分子生物学检查等。
3. 淋巴细胞
使用反应性淋巴细胞描述因良性病因而产生形态学变化的淋巴细胞,使用异常淋巴细胞并附以相应的形态学特征来描述因可疑恶性或克隆性病因而产生肿瘤性变化的淋巴细胞。[注:欧洲白血病网(European leukemia net,ELN)2010年的共识中提到,基于形态学可将不典型淋巴细胞(atypical lymphocyte)进一步划分为:①不典型淋巴细胞‑疑为反应性;②不典型淋巴细胞‑疑为肿瘤性;③不典型淋巴细胞‑性质不确定。ICSH指南中采纳了这一分类建议,这种分类方式涵盖了形态学者的综合判断,对疾病可能的性质具有指导作用,亦在本指南中给予推荐。]
(1)反应性淋巴细胞:
当外周血涂片中出现反应性淋巴细胞时应进行分类计数;当反应性淋巴细胞≥10%时,层次2可描述为“请结合临床以除外传染性单个核细胞增多症可能”,层次3可建议进行病毒感染相关检测。反应性淋巴细胞的形态变化主要包括细胞体积增大,细胞边缘不规则、深染可出现“裙边”现象;胞浆量更丰富、着色从浅蓝色到深蓝色不等;胞核亦可呈不规则形,染色质松散不够致密。
(2)异常淋巴细胞:
主要包括毛细胞、幼淋巴细胞、脑回状核淋巴细胞、花形核淋巴细胞及骨髓瘤细胞等各种类型淋巴瘤细胞以及白血病性原始淋巴细胞等。
在白细胞分类计数时应单独给出该类细胞的百分比,如少量偶见,也应在描述性报告中予以说明。
①对于免疫表型分析未确诊的某些淋巴瘤细胞,推荐在白细胞分类时以“异常淋巴细胞”进行单独分类计数并在描述性报告中进行形态描述。
②对于外周血中出现的骨髓瘤细胞、幼淋巴细胞,建议在白细胞分类计数时按其具体细胞名称进行单独分类计数。
③由于原始淋巴细胞在形态上不易与髓系原始细胞以及淋巴瘤细胞等相鉴别,故建议在白细胞分类计数时将原始淋巴细胞以“原始细胞”进行分类计数。
描述性报告中,层次1主要是对该类细胞做一个形态学特征的简明描述,可参考以下内容:①细胞大小;②核浆比例;③核:核染色质的性质(细致、粗糙)及结构(致密、疏松)、核型(规则或不规则)、核仁有无;④胞浆(绒毛、颗粒、空泡及着色等)。在层次2中可给出一至两个倾向性诊断建议。层次3一般建议进一步行病理活检、免疫表型分析、骨髓细胞学检查、细胞遗传学检查或分子生物学检查等。
(3)对于无特征形态和(或)不确定性质的淋巴细胞增多,如伴有大颗粒淋巴细胞增多或双核淋巴细胞存在时,因缺乏精确的临床诊断信息,或不确定其良恶性,应在描述性报告的层次1中强调成熟淋巴细胞增加并描述观察到的形态;无层次2的描述;层次3的描述可根据具体情况而定,建议随访或进一步鉴别诊断的措施如免疫表型分析。
(4)涂抹细胞:
在淋巴细胞增殖性疾病等患者的外周血涂片中可能会看到较多的涂抹细胞,建议在这种情况下可报告仪器自动分类结果,但需对涂抹细胞给予适当描述说明。
4. 单核细胞
(1)幼稚单核细胞:
血涂片中发现幼稚单核细胞时,应对其单独分类计数并在描述性报告中给予说明。结合临床信息,如为诊断AML或CMML时,外周血中幼稚单核细胞应等同计数为原始细胞。如实际工作中形态上和原始单核细胞较难明确鉴别时,可与原始单核细胞一并归为“原幼单核细胞”或“原幼细胞”进行分类计数。
(2)异常单核细胞:
目前仍推荐将其作为单核细胞进行分类计数,但需对其形态在描述性报告中给予描述说明。[注:在使用G‑CSF生长因子治疗或骨髓应激情况以及某些造血系统恶性肿瘤(尤其是CMML)时,外周血中的成熟单核细胞亦可出现形态改变,称为异常单核细胞。这些单核细胞的体积较原始单核细胞及幼稚单核细胞更大、胞浆更丰富、核形扭曲凹陷折叠更加明显,核染色质偏细致但更趋于成熟。]
(3)在描述性报告中,层次1主要描述单核细胞的形态,有无发育不良的单核细胞及未成熟细胞的出现(原始单核细胞、幼稚单核细胞)。在缺少典型的形态学证据支持时,层次2及3的描述则限于“单核细胞增多,建议随访”或缺省。
5. 原始细胞
(1)血涂片中出现原始细胞,即使很少的数量,也需要做到:
①知悉临床相关情况(如怀疑造血系统疾病、已知疾病的随访、化疗间隔的时间以及是否使用生长因子);
②仔细观察原始细胞的形态,是否有恶性肿瘤的特征、核异形(轮廓不规则、“杯口”样核)或胞质异常(Auer小体、胞质深染且有蜂窝样空泡等)。
(2)由于形态学的异质性,原始淋巴细胞、原始粒细胞、原始单核细胞及原始巨核细胞等均推荐归为“原始细胞”进行分类计数。幼稚单核细胞及异常早幼粒细胞可视为“原始细胞”,尤其异常早幼粒细胞需要单独进行分类计数并及时报告临床。
(3)在描述性报告中,层次1需对原始细胞进行形态描述,注重是否有髓系分化(粒或单核)的迹象以及有无Auer小体(单个或柴捆状)等;层次2可以笼统分型(怀疑急性白血病、AML 或 MDS)也可以精确分型(如急性早幼粒细胞白血病);层次3明确需采取的措施,通常建议进一步行骨髓细胞学检查、免疫表型分析、细胞遗传学检查或分子生物学检查等,以及作为危急值报告临床需紧急采取治疗措施(如急性早幼粒细胞白血病)。
6. 形态学无法分类的细胞或异常细胞
(1)某些情况下,不能单以形态学特征来确定异常细胞的系别和分化阶段,此时可使用“分类不明细胞”或“形态异常细胞”来进行分类报告。
(2)在描述性报告中,层次 1 中需对该类细胞的形态学特征给予描述。在层次3的描述中可建议对该类细胞进行进一步的鉴定,尤其是免疫表型分析。
(三)血小板
1. 当血小板计数异常时,血小板相关的形态异常更具有临床意义。在对血小板异常形态进行描述性报告时,可在层次1中对血小板的大小(是否有血小板大小不等、小血小板、大血小板及巨血小板等)、形状、颗粒(是否少或缺颗粒)以及分布情况进行适当描述,对巨大血小板需采用分级方式进行报告;适用时,在层次2中可结合血小板计数结果提示1~2个可能的诊断方向并在层次3中针对进一步的检查给予适当的建议,参见表3。
应用血液分析仪进行血小板检测时,应注意血小板计数结果及异常报警,需识别标本是否存在干扰血小板计数的因素(如血液凝固、血小板聚集、血小板卫星现象、冷球蛋白、细胞碎片等)并及时进行处理,必要时在报告中增加包括血小板形态在内的相关描述。在某些疾病中,如 MDS 或某些慢性或急性髓系白血病,虽可观察到血小板形态的异常,但相比合并的其他血细胞异常其临床价值可能不是首要的,这时对于显著的血小板形态异常可在层次1中给予适当描述。
2. 正常外周血中几乎见不到巨核细胞(新生儿除外)。但在病理情况下,如一些血液肿瘤患者的外周血涂片中可能会见到小巨核以及巨核细胞祼核等,这时亦需要给予适当的描述。
(四)两系或全血细胞减少
首诊时,两系或全血细胞减少可能的情况包括骨髓造血功能异常、外周血细胞破坏过多或分布异常等,须查找是否存在异常细胞并加以描述说明。
四、检验与临床沟通
1. 紧急情况的处理:
对于紧急情况,应及时通知临床医生,包括危急值的报告以及其他需与临床医生沟通的特殊情况。除数值异常的危急值外,其他需联系临床医生的紧急情况包括:初发急性白血病尤其是急性早幼粒细胞白血病,血栓性微血管病如TTP、HUS及DIC等。如发现血液寄生虫,如疟原虫、巴贝虫等,应按寄生虫传报制度执行。
2. 报告发布与结果解释:
报告内容应考虑结果的临床相关性,应对有临床价值的信息给予综合描述,描述内容应清晰明了,明显异常的结果可由临床医生向患者给予充分解释。
